Eversense ซึ่งเป็นเครื่องตรวจน้ำตาลกลูโคสแบบต่อเนื่อง (CGM) ที่ฝังได้เป็นครั้งแรกกำลังจะกลับมาอีกครั้งหลังจากผู้ผลิต Senseonics เกือบจะท้องอืดเนื่องจากวิกฤต COVID-19 ด้วยการจ่ายเงินสดจำนวนมากจาก Ascensia Diabetes Care ยักษ์ใหญ่ด้านเภสัชกรรม .
Senseonics ถูกบังคับให้หยุดการขายเครื่องมือรักษาโรคเบาหวานที่ไม่เหมือนใครนี้ในช่วงปลายเดือนมีนาคมโดยจะเข้าสู่ "โหมดจำศีล" เนื่องจากรอการลงทุนหรือการเป็นหุ้นส่วนที่เหมาะสมตามที่หัวหน้าเจ้าหน้าที่การแพทย์ดร. Francine Kaufman กล่าว
ขณะนี้พระคุณการประหยัดได้มาถึงในรูปแบบของข้อตกลงการค้าและการทำงานร่วมกันกับ Ascensia ซึ่งเป็นผู้ผลิตเครื่องวัดระดับน้ำตาลในนิ้วมือจากสวิตเซอร์แลนด์ซึ่งเดิมชื่อไบเออร์ ข้อตกลงดังกล่าวให้สิทธิ์การจัดจำหน่ายทั่วโลก แต่เพียงผู้เดียวของ Ascensia สำหรับผลิตภัณฑ์ Eversense CGM ในปัจจุบันและอนาคตเป็นเวลาอย่างน้อย 5 ปีข้างหน้า
เซ็นเซอร์ Eversense ปัจจุบันได้รับการอนุมัติให้ใช้งานได้เพียง 3 เดือนซึ่งหลายคนเชื่อว่าเป็นช่วงเวลาสั้นเกินไปสำหรับบางสิ่งที่ต้องใช้แผลผ่าตัด แต่ Senseonics ซึ่งตั้งอยู่ในรัฐแมรี่แลนด์คาดว่าจะยื่นฟ้องต่อสำนักงานคณะกรรมการอาหารและยา (FDA) ในระยะเวลา 6 เดือนซึ่งเป็นที่คาดหวังไว้สูง“ เร็ว ๆ นี้” ดังนั้น Ascensia จึงพร้อมที่จะแข่งขันในตลาด CGM
โรคระบาด
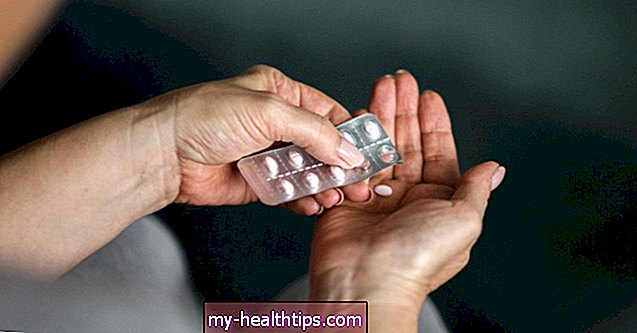
ความจำเป็นในการผ่าตัดเล็กทุก ๆ 90 วันเพื่อใส่เซ็นเซอร์ Eversense ใต้ผิวหนังนั้นเป็นเรื่องยากสำหรับผู้ป่วยบางราย แต่เมื่อการแพร่ระบาดทั่วโลกทำให้ผู้ให้บริการยกเลิกการนัดหมายด้วยตนเองส่วนใหญ่ Eversense ก็ประสบปัญหาอย่างหนัก เช่นเดียวกับที่ บริษัท เริ่มได้รับแรงฉุด - และเช่นเดียวกับที่พวกเขาปิดข้อตกลงสำหรับการรายงานข่าวของ Medicare นักลงทุนของพวกเขาก็ดึงปลั๊กออกตามที่ Kaufman กล่าว
แต่ข้อตกลง Ascensia นี้ทำให้ บริษัท มีลูกกลอนทางการเงินช่วยชีวิตจำนวน 35 ล้านดอลลาร์ในตอนนี้และอีก 15 ล้านดอลลาร์เมื่อผลิตภัณฑ์ Eversense XL 180 วันได้รับการอนุมัติจาก FDA
นอกเหนือจากเซ็นเซอร์ 90 วันที่ได้รับการอนุมัติในปัจจุบันและ Eversense XL ที่กำลังจะมาถึงในที่สุด Ascensia จะช่วยขายเซ็นเซอร์ฝังตัว 365 วันในอนาคตที่อยู่ระหว่างการพัฒนา
Ascensia จะขายเทคโนโลยี Eversense CGM
ข้อตกลงการจัดจำหน่ายเฉพาะทั่วโลกนี้คาดว่าจะมีผลจนถึงปี 2568 ตั้งแต่ปลายปี 2020 เราจะเริ่มเห็นชื่อของ Ascensia แนบไปกับกิจกรรมทางการตลาดและการขายบางอย่างสำหรับผลิตภัณฑ์ Eversense CGM ในยุโรป Ascensia จะเริ่มวางจำหน่ายผลิตภัณฑ์ Eversense เมื่อความร่วมมือด้านการจัดจำหน่ายที่มีอยู่ได้ข้อสรุป
ในขณะนี้ชื่อแบรนด์ Senseonics และ Eversense จะยังคงอยู่ Ascensia กล่าวว่าพวกเขากำลัง“ ทำงานร่วมกับ Senseonics เพื่อตรวจสอบวิธีที่เราสามารถรวมชื่อ Ascensia ได้ แต่เราไม่สามารถยืนยันได้ว่าจะทำอย่างไรในขั้นตอนนี้”
Ascensia จะเข้ารับช่วงการสนับสนุนลูกค้าเมื่อได้รับสิทธิ์ในการจัดจำหน่ายในแต่ละตลาด - สหรัฐอเมริกาในไตรมาสที่ 4 ปี 2563 เยอรมนีอิตาลีสวิตเซอร์แลนด์ในไตรมาสที่ 1 ปี 2564 และสวีเดนในไตรมาสที่ 4 ปี 2564 สำหรับการแก้ไขปัญหาพวกเขาจะ "ดึงข้อมูลจาก Senseonics หากจำเป็น"
ในเดือนสิงหาคม 2020 ผู้ให้บริการด้านการดูแลสุขภาพจำนวนมากที่ไม่สามารถดำเนินการขั้นตอนการสอดใส่ได้กลับมาดำเนินการได้ ดังนั้น Senseonics ส่วนใหญ่ได้กล่าวถึงงานที่ค้างอยู่ Kaufman กล่าว บริษัท ได้รับการติดต่อและได้รับการติดต่อจากผู้ใช้หลายราย แต่ถ้าใครยังมีปัญหาอยู่ก็แนะนำให้ติดต่อ Senseonics โดยตรง
เตรียมพร้อมสำหรับการซื้อกิจการ?
แม้ว่าข้อตกลงปัจจุบันนี้จะไม่ใช่การควบรวมกิจการหรือการเข้าซื้อกิจการ แต่ก็ดูเหมือนเป็นทิศทางที่ Ascensia กำลังมองหา
“ ความร่วมมือครั้งนี้ถือเป็นก้าวต่อไปในการสร้างแฟรนไชส์การดูแลผู้ป่วยเบาหวานระดับโลกสำหรับ Ascensia เนื่องจากเรามุ่งหวังที่จะขยายธุรกิจของเรานอกเหนือจากการตรวจระดับน้ำตาลในเลือด (แบบแท่งนิ้ว)” Robert Schumm ประธาน Ascensia Diabetes Care และผู้อำนวยการจัดการโรคเบาหวานกล่าว “ มันจะช่วยให้เราสามารถสร้างสถานะในตลาด CGM โดยเฉพาะในสหรัฐอเมริกาและยุโรปและจะเพิ่มความแข็งแกร่งให้กับกลุ่มผลิตภัณฑ์ที่มีอยู่ของเรา”
“ เราเชื่อว่าการผสมผสานระหว่างความเชี่ยวชาญเชิงพาณิชย์และโครงสร้างพื้นฐานควบคู่ไปกับการพัฒนาผลิตภัณฑ์และความเชี่ยวชาญทางคลินิกของ Senseonics จะช่วยให้ผลิตภัณฑ์ Eversense และ Eversense XL อยู่ในมือของผู้ป่วยโรคเบาหวานที่จะได้รับประโยชน์จากผลิตภัณฑ์เหล่านี้ เป้าหมายของเราคือการทำงานร่วมกันเพื่อนำเทคโนโลยีที่มีประสิทธิภาพสูงเหล่านี้มาสู่ผู้ป่วยโรคเบาหวานจำนวนมากขึ้นดังนั้นจึงเป็นทางเลือกเพิ่มเติมใน CGM สำหรับการจัดการโรคเบาหวาน” Schumm กล่าวเสริม
แม้ว่าการซื้อกิจการในอนาคตจะไม่ได้อยู่ในผลงาน แต่สิ่งนี้ก็ยังคงเป็นประโยชน์อย่างมากสำหรับ Senseonics ซึ่งต้องดิ้นรนตั้งแต่ได้รับการอนุมัติจาก FDA เป็นครั้งแรกสำหรับเซ็นเซอร์ที่ฝังในปี 2018 การเปิดตัวแอปตรวจสอบระยะไกลในเดือนพฤษภาคม 2020 ทำให้ระบบมีประสิทธิภาพมากขึ้น เสร็จสมบูรณ์
.jpg)








.jpg)